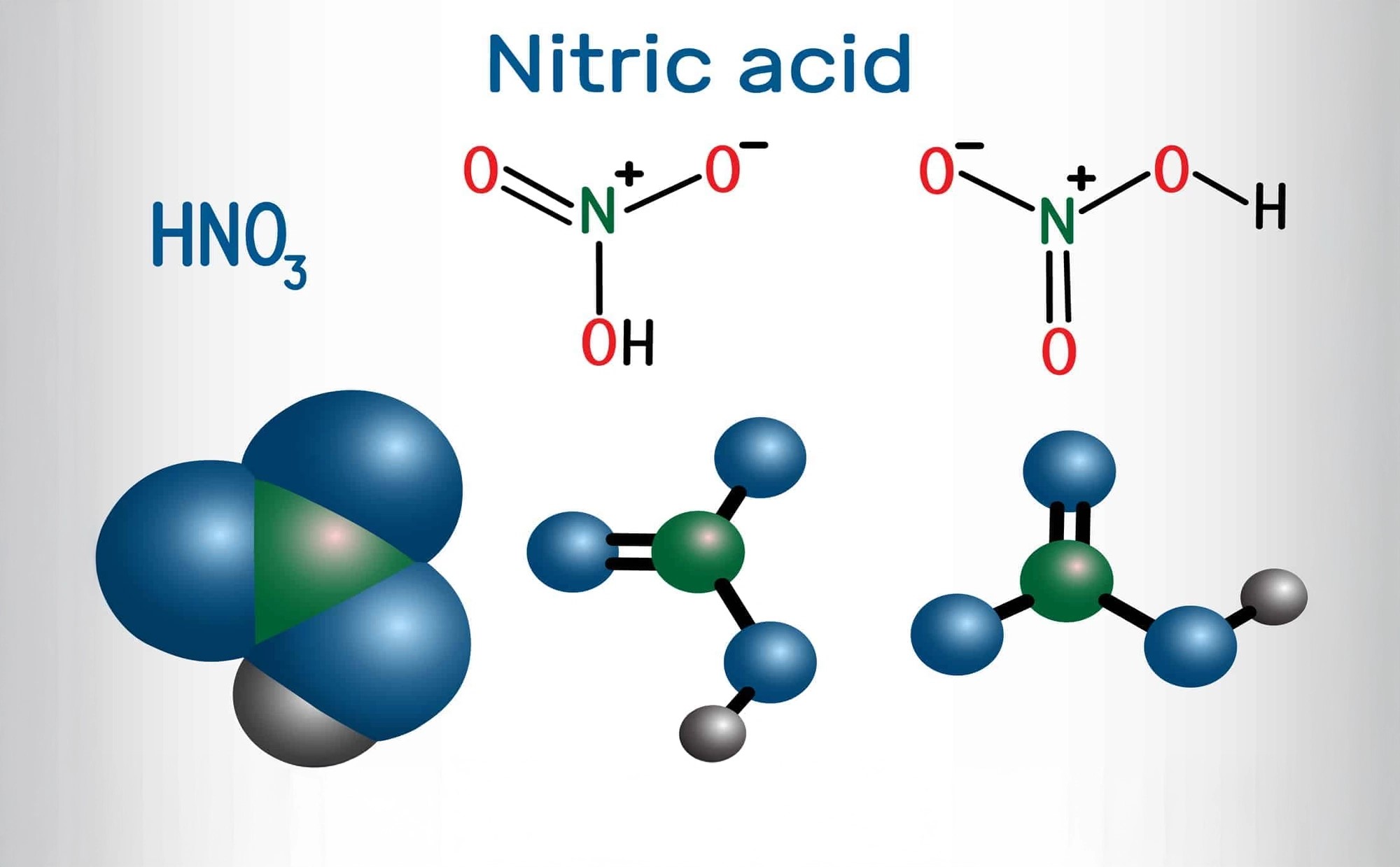
Nitrik asit ( Nitric acid 50-55 % )
$10,00
Bu ürün yüsek risk grubunda olduğunda dolayı kargo ile gönderimi yapılmamaktadır.
Kimyasal özellikler: Nitrik asit, HN03, güçlü, yangın tehlikesi olan bir oksidandır. Su ile karışabilen ve 86 ℃ (187 ℉) sıcaklıkta kaynayan renksiz veya sarımsı bir sıvıdır. Aqua fortis olarak da bilinen nitrik asit, kimyasal sentez, patlayıcılar ve gübre üretimi için ve metalürji, dağlama, gravür ve cevher yüzdürmede kullanılır. Nitrik asit, keskin, boğucu bir kokuya sahip, renksiz ila açık kahverengi dumanlı bir sıvıdır. Dumanlı nitrik asit kırmızımsı dumanlı bir sıvıdır. Nemli havada dumanlar. Genellikle sulu bir çözelti içinde kullanılır. Dumanlı nitrik asit, çözünmüş nitrojen dioksit içeren konsantre nitrik asittir. Nitrik asit, sudaki bir nitrojen dioksit, NO2 çözeltisidir ve dumanlı nitrik asit olarak adlandırılan, fazla miktarda NO2 içerir ve sarı ila kahverengimsi-kırmızı renktedir. Reaktivite Profili:Nitrik asit; alkoller, aminler, amonyak, berilyum alkiller, boranlar, disiyanojen, hidrazinler, hidrokarbonlar, hidrojen, nitroalkanlar, toz metaller, silanlar veya tiyoller ile temas ettiğinde tutuşur [Bretherick 1979. s.174]. İnce taneli antimon ve nitrik asidin reaksiyonu şiddetli olabilir [Pascal 10:504. 1931-34]. Brom pentaflorür güçlü nitrik asit ve güçlü sülfürik asitle şiddetli reaksiyona girer [Mellor 2, Ek. 1:172. 1956]. Deneyler, asetik anhidrit içinde ağırlıkça %50’den fazla nitrik asit karışımlarının infilaklı patlayıcılar olarak işlev görebileceğini göstermektedir [BCISC 42:2. 1971]. Eşit oranlarda aseton, nitrik asit ve %75 asetik asitten oluşan bir dağlama maddesi, Nitrik asit hazırlanıp kapalı bir şişeye yerleştirildikten 4 saat sonra patladı. Bu, hassas bir patlayıcı [Chem. Müh. Haber 38: 56. 1960]. Fosfin, konsantre nitrik asit tarafından şiddetli bir şekilde ayrışır ve alev üretilir. Sıcak dumanlı nitrik asit, bir fosfin gazı kabına atıldığında bir patlama meydana getirir [Edin. Roy. Sos. 13:88. 1835]. Nitrik asit fosfor triklorür [Comp. Parçala. 28:86]. Sodyum azid ve güçlü nitrik asidin reaksiyonu enerjiktir [Mellor 8, Ek 2:315. 1967]. Isı, duman ve sıçrama üretimi ile su ile şiddetli reaksiyona girer. Sodyum azid ve güçlü nitrik asidin reaksiyonu enerjiktir [Mellor 8, Ek 2:315. 1967]. Isı, duman ve sıçrama üretimi ile su ile şiddetli reaksiyona girer. Sodyum azid ve güçlü nitrik asidin reaksiyonu enerjiktir [Mellor 8, Ek 2:315. 1967]. Isı, duman ve sıçrama üretimi ile su ile şiddetli reaksiyona girer. Sağlık tehlikesi:Nitrik asit ciltte sarı yanıklara neden olan aşındırıcı bir maddedir. Karmaşık proteinleri ksantoproteikasit adı verilen sarı bir maddeye dönüştürerek vücut dokularını aşındırır (Meyer 1989). Asidin yutulması ağızda ve midede yanmaya ve aşınmaya neden olabilir. 5-10 mL’lik bir doz insanlar için ölümcül olabilir. Nitrik asidin buharına ve buğusuna kronik olarak maruz kalmak bronşite ve kimyasal pnömoniye neden olabilir (Fairhall 1957). Işık varlığında ayrışmasıyla oluşan oldukça zehirli bir gaz olan NO2 yayar. Nitrik asit, sülfürik asitten daha az aşındırıcıdır. Buharı ve buğusu dişleri aşındırabilir. Yanıcılık ve Patlayabilirlik: Patlayabilirlik Yanıcı bir madde değil, güçlü bir oksitleyicidir. Pek çok organik madde dahil olmak üzere kolayca oksitlenebilen malzemelerle temas, yangın veya patlamalara neden olabilir. Atık Bertarafı:Sodyum ve kalsiyum nitratın nötr çözeltisini oluşturmak için soda külü ile sönmüş kireç eklenir. Bu çözelti su ile seyreltildikten sonra boşaltılabilir. Ayrıca nitrik asit geri kazanılabilir ve bazı durumlarda akrilik elyaf döndürme solüsyonlarında olduğu gibi yeniden kullanılabilir. Kabul edilebilir imha uygulamaları hakkında rehberlik için çevre düzenleyici kurumlara danışın. Bu kirletici maddeyi (≥100 kg/mo) içeren atık üreticileri, depolama, nakliye, arıtma ve atık bertarafını yöneten EPA düzenlemelerine uymalıdır.
| Litre | 5 lt |
|---|
There are no reviews yet.