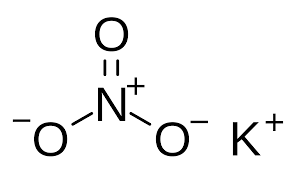
Potasyum nitrat ( Potassium nitrate )
₺10,00
- KNO3 99,7 % min.
- pH 6,0 – 8,5
- Na 300 ppm max.
- Ca 8 ppm max.
- Mg 8 ppm max.
- Fe 10 ppm max.
- Cl 350 ppm max.
- Insolubles 500 ppm max.
- M 101 g/mol
- Melting point 335 C
- Solub. İn water 320 g/l
- CAS No 7757-79-1
Kimyasal özellikler : Potasyum nitrat, 337°C’de eriyen, kokusuz, yanıcı, suda çözünebilen, tuzlu tadı olan beyaz veya renksiz kristallerdir. Piroteknikte, patlayıcılarda ve kibritlerde gübre olarak ve analitik reaktif olarak kullanılır. Fiziki ozellikleri : Renksiz şeffaf kristaller veya beyaz granül veya kristal toz; eşkenar dörtgen yapı; yoğunluk 2,11 g/cm3, 20 °C’de; 334°C’de erir; 400°C’de oksijeni geliştirerek ayrışır; soğuk suda çözünür, 0°C’de 13,3 g/100mL; kaynar suda yüksek oranda çözünür, 100°C’de 247 g/100mL; çözünme sırasında suyun sıcaklığını düşürür; etanolde çok az çözünür; Gliserol ve sıvı amonyakta çözünür. Kullanım Alanları : Güherçilenin en belirgin kullanımı kara barut üretimi olsa da, gübre olarak da potasyum nitrat kullanılıyor. 17. yüzyılın ilk yarısında Johann Rudolf Glauber (1604–1668) hayvan ağıllarından güherçile elde etti ve bunun bitki büyümesini desteklemek için kullanımını keşfetti. Glauber gübre karışımlarına güherçileyi diğer besinlerle birlikte ekledi. Glauber’in çalışması bitki beslenmesinde besin döngüsünün önemini gösteren ilk çalışmalardan biriydi. Bu doğal madde kireç ve idrarın ayrışmasının ürünüdür. Beyaz granüller veya toz suda 1:3 oranında çözünür, ancak alkolde çözünmez. Güherçile veya nitre olarak da adlandırılan potasyum nitrat, kolodyum üretimi için sülfürik asit ile pamuğu nitratlamak üzere birleştirildi. Ayrıca flaş tozu yapmak için magnezyum ile birlikte kullanıldı ve kolodyum pozitiflerinde soğuk beyaz tonlar üretmek için demir sülfat geliştiricilere eklendi. Havai fişeklerde, fluxlarda, salamura etlerde; nitrik asit üretimi; cam, kibrit, barut imalatı; karışımların dondurulması. Tarımsal gübre. Gıdalarda koruyucu. Diş aşırı hassasiyetini azaltmak için diş macunlarında. Dünya Sağlık Örgütü (WHO) : Potasyum nitrat eskiden idrar söktürücü olarak kullanılıyordu. Bu amaçla kullanımının artık geçerliliğini yitirdiği düşünülüyor ancak en az bir ülkede potasyum eksikliğinin düzeltilmesi için hâlâ mevcut. Tescilli diş macunlarında da %5 düzeyindeki konsantrasyonlara yaygın olarak izin verilmektedir. Nitratların aşırı kullanımı ve bunların nitrozaminlere dönüşmesinden kaynaklanan potansiyel kanserojen risk nedeniyle bazı ülkelerde ilaç yasaklanmıştır. Uyumsuzluklar : Güçlü bir oksitleyici. Organik malzemelerle ve birçok malzemeyle karıştırıldığında tehlikeli derecede reaktif, sürtünmeye ve darbeye duyarlı. İndirgeyici maddelerle şiddetli reaksiyonlar; kimyasal olarak aktif metaller; kömür, trikloroetilen. Güvenlik profili : İntravenöz yolla zehir. Yutulması halinde orta derecede toksiktir. Deneysel bir teratojen. Deneysel üreme etkileri. Mutasyon verileri rapor edildi. Büyük miktarlarda yutulması gastroenterite neden olabilir. Kronik maruz kalma anemi, nefrit ve methemoglobinemiye neden olabilir. Isıtıldığında kalsiyum hidroksit + poliklorlu fenollerle reaksiyona girerek son derece toksik klorlu benzodtoksinler oluşturur. Güçlü bir oksitleyici. Barut, potasyum nitrat + kükürt + odun kömürünün bir karışımıdır. Alüminyum + baryum nitrat + potasyum perklorat + su (depoda), bor + laminak + trikloroetilen ile patlayıcı reaksiyon. Laktoz, toz metaller (örneğin titanyum, antimon, germanyum), metal sülfürler (örneğin antimon trisülfür, baryum sülfür, kalsiyum sülfür, germanyum monosülfür, titanyum disülfür, arsenik disülfür, molibden disülfür), ametaller (örneğin boron) ile patlayıcı karışımlar oluşturur , karbon, beyaz fosfor, arsenik), organik materyaller, fosfitler (örn., bakır(l1) fosfit, bakır monofosfit), indirgeyici maddeler (örn., sodyum fosfinat, sodyum tiyosülfat), sodyum asetat. Uygun koşullar altında 1,3-bis(trikloromet~d)benzen, bor fosfat, F2, kalsiyum shcid, kömür, krom nitrür, Na hipofosfat, ma2O2 + dekstroz), kırmızı fosfor, (S + As2S3), ile şiddetli reaksiyona girebilir, toryum dikarbit, trikloroetilen, çinko, zirkonyum. Ayrışıncaya kadar ısıtıldığında çok zehirli NOx ve K2O dumanları yayar.
| Ağırlık | 1 kg |
|---|
There are no reviews yet.