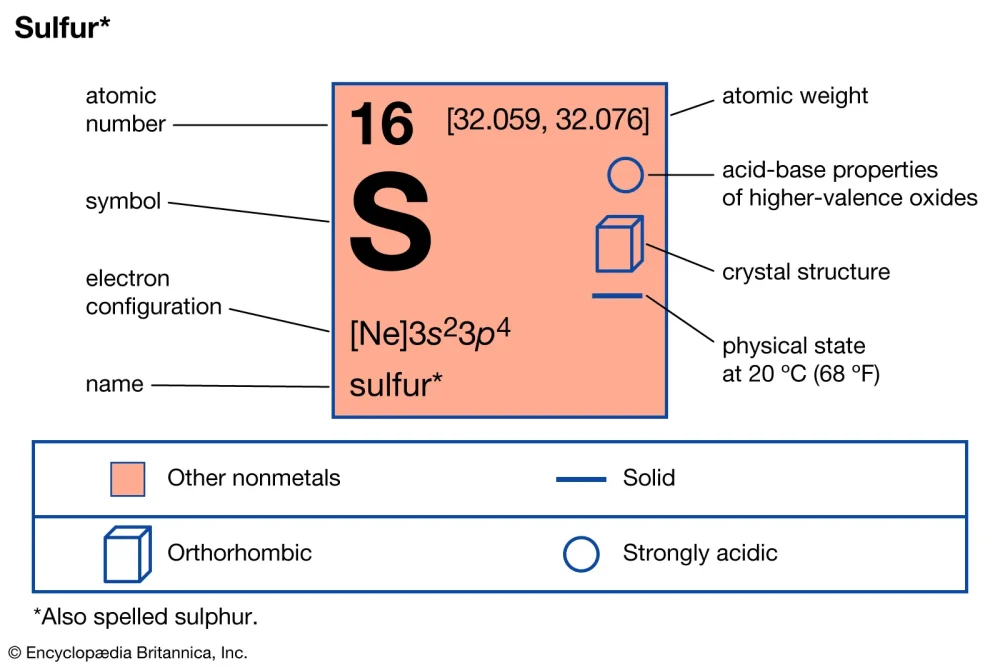
Kükürt çöktürülmüş ( Sulphur precipitated )
₺5,00
- Assay 99,9 %
- Density 1.9 g/cm3
- Solub. in water insoluble
- Flash point 195 0C
- M 32.06 g/mol
- Melting point 115 0C
- Boiling point 444 0C
- Ignition temp 235 0C
- CAS No. 7704-34-9
Kimyasal Özellikler] Sülfür, S, kristal veya amorf formda ve dört kararlı izotopta bulunan metalik olmayan bir elementtir. Kükürt, eşkenar dörtgen form için 112,8°C (234 °F) ile amorf kükürt için 120,0°C (248 °F) arasında değişen sıcaklıklarda erir ve tüm formlar 444,7°C’de (835°F) kaynar. Kükürt, birçok volkanik bölgede serbest kükürt olarak bulunur ve genellikle jips ve kireçtaşı ile ilişkilidir. Kimyasal ara madde ve fungisit olarak ve kauçuğun vulkanizasyonunda kullanılır. [İzotoplar] Kükürtün toplam 24 izotopu vardır; bunların dördü hariç hepsi radyoaktiftir. Dört kararlı izotop ve bunların Dünya’daki toplam kükürt bolluğuna katkıları şu şekildedir: S-32, kükürt bolluğuna %95.02 katkıda bulunur; S-33, sadece %0,75; S-34,4.21%; ve S-36, %0,02. [Sağlık Tehlikesi] Göz tahrişine neden olabilir; cildi nadiren tahriş edebilir. Geri kazanılmış kükürt varsa, hidrojen sülfite bakın.* [Potansiyel Maruz Kalma] Sülfürik asit üretiminde yaygın olarak kullanılır; karbon bisülfür; ilaçlar, fungisitler, barut, odun hamuru; kauçuk ve diğer ürünler. [İlk yardım] Bu kimyasal göze kaçarsa, kontakt lensleri hemen çıkarın ve hemen en az 15 dakika yıkayın, ara sıra üst ve alt göz kapaklarını kaldırın. Derhal tıbbi yardım alın. Bu kimyasal ciltle temas ederse, kirlenmiş giysileri çıkarın ve hemen sabun ve su ile yıkayın. Derhal tıbbi yardım alın. Bu kimyasal solunmuşsa, maruziyetten uzaklaştırın, solunum durmuşsa kurtarıcı solumaya (evrensel önlemleri kullanarak, resüsitasyon maskesi dahil) başlayın ve kalp hareketi durmuşsa CPR’ye başlayın. Derhal tıbbi bir tesise transfer edin. Bu kimyasal yutulduğunda tıbbi yardım alın. Bol miktarda su verin ve kusturun. Bilinci yerinde olmayan kişiyi kusturmayın. [Uyumsuzluklar] Sülfürik asit üretiminde yaygın olarak kullanılır; karbon bisülfür; ilaçlar, fungisitler, barut, odun hamuru; kauçuk ve diğer ürünler. [Tehlike] Kükürt bileşiklerinin çoğu zehirlidir ancak yaşam için gereklidir. Elementel kükürtten ve kükürt bileşiklerinin çoğundan çıkan gaz, solunduğunda zehirlidir ve yutulduğunda ölümcüldür. Kükürt bileşiklerinin sıçan ve farelerin yok edilmesinde etkili olmasının yanı sıra insektisitlerin bir bileşeni olmasının nedeni budur. Sülfa ilaçları (sülfanilamid ve sufadiazin) toksik olmasına rağmen penisilin gelişmeden önce. [Kullanımlar] Elemental kükürt kauçuğu vulkanize etmek için kullanılır; siyah barut yapmak; toprak düzenleyici olarak; bir fungisit olarak; bir dizi metal sülfürün hazırlanması; ve karbon disülfid üretmek. Maçlarda da kullanılır; odun hamuru, saman, ipek ve yünün ağartılması; ve birçok boyanın sentezinde. Farmasötik dereceli çökeltilmiş ve süblimleştirilmiş kükürtler, losyonlarda ve merhemlerde kabuk öldürücüler ve antiseptikler olarak kullanılır. Önemli kükürt bileşikleri arasında sülfürik asit, kükürt dioksit, hidrojen 890 SULFUR sülfit, kükürt trioksit ve bir dizi metal sülfür ve sülfatlar, bisülfatlar ve sülfitler gibi metal okso-tuzları bulunur. Merkaptanlar, tiyofenler, tiyofenoller, sülfat esterler, sülfonlar ve karbon disülfid gibi çok sayıda organik bileşik kükürt içerir. [Reaksiyonlar] Kükürt iki oksit oluşturur, kükürt dioksit, SO2 ve trioksit, SO3. Oksijende yaklaşık 250°C’de veya 260°C’nin üzerindeki havada yanarak kükürt dioksit oluşturur. Fazla oksijende trioksit elde edilir. Kükürt, hidrojen ile 260 ila 350°C’de reaksiyona girerek hidrojen sülfit oluşturur. Reaksiyon bu sıcaklıkta yavaştır ve tamamlanmaz. Reaksiyon, aktif alümina ile katalize edilir. Fazla klor veya flor ile reaksiyonlar kükürt tetraklorür, SCl4 veya hekzaflorür, SF6 verir. Bu reaksiyonlar soğuk koşullar altında gerçekleşir. Kükürt, disülfüroksit S2O oluşturmak için bir elektrik deşarjında kükürt dioksit ile reaksiyona girer. Sülfür sulu sülfid ile reaksiyona girerek polisülfitler oluşturur: S + Na2S → Na2S2 Sulu sülfit çözeltisi ile ürün tiyosülfattır: S + SO32– → S2O32– Tiyosülfat ayrıca kükürdün toz sülfit ile ısıtılmasıyla elde edilir:S + Na2SO3 → Na2S2O3Alkali siyanür ile ısıtıldığında tiyosiyanat tuzu elde edilir: S + KCN → KSCN
Benzer bir reaksiyon, tiyosiyanatın içinde bulunduğu sulu fazda meydana gelir. buharlaştırma ve kristalleştirme ile elde edilir.
| Ağırlık | 25 kg, 1 kg |
|---|
There are no reviews yet.